
پژوهشگران دانشگاه شیکاگو روش نوینی برای درمان سرطان با استفاده از نانوذرات ابداع کردند
به گزارش گروه دانشگاه خبرگزاری دانشجو به نقل از ستاد نانو؛ پژوهشگران روشی ابداع کردهاند که با کمک نانوذرات، داروهای ضدسرطان را فقط در محل تومور رها میکند و به بافتهای سالم آسیبی نمیزند. این روش، عوارض داروهای شیمیدرمانی را کاهش میدهد و اثربخشی آنها را بالا میبرد. نکتهی مهم اینجاست که این نانوذره به شرایط شیمیایی خاص تومور واکنش نشان میدهد، نه کل بدن!
پژوهشگران مرکز جامع سرطان دانشگاه شیکاگو (University of Chicago Medical Center) با طراحی سامانهای نوآورانه برای رسانش هدفمند داروهای ضدسرطان با بهرهگیری از نانوذرات، گامی مؤثر در کاهش عوارض جانبی و افزایش کارایی شیمیدرمانی برداشتهاند. این دستاورد میتواند تحولی چشمگیر در درمانهای سرطانی ایجاد کند.
در گزارشی تازه که در نشریهی معتبر Cell Reports Medicine به چاپ رسیده، گروهی از دانشمندان دانشگاه شیکاگو موفق به طراحی سامانهای مبتنیبر نانوذرات شدهاند که داروی ضدسرطان را بهگونهای هدفمند به سلولهای توموری میرساند و از آسیبرسانی به بافتهای سالم بدن جلوگیری میکند. این فناوری نهتنها به پزشکان امکان میدهد دُز بیشتری از دارو را بدون نگرانی از عوارض جانبی تجویز کنند، بلکه میزان اثربخشی درمان را نیز بهطور چشمگیری افزایش میدهد.
یکی از چالشهای دیرین درمان سرطان، دشواری در تمایز سلولهای سرطانی از سلولهای طبیعی بدن است. سلولهای سرطانی با زیرکی از دید سیستم ایمنی میگریزند و بسیاری از درمانها به دلیل نگرانی از آسیب به سلولهای سالم، در دُزهای پایینتری تجویز میشوند که از اثرگذاری آنها میکاهد.
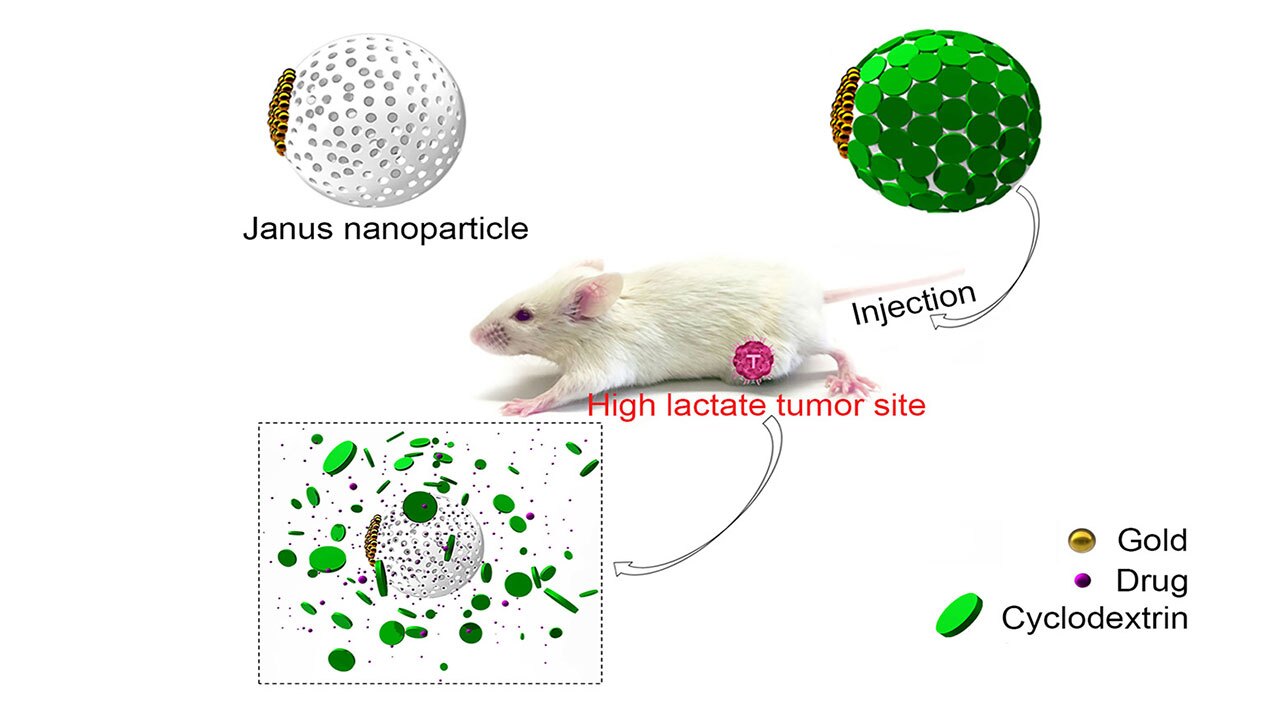
دانشمندان این پژوهش برای حل این معضل، از پدیدهای زیستی بهنام «اثر واربرگ» بهره گرفتند؛ پدیدهای که به تفاوت نحوهی مصرف قند (گلوکز) در سلولهای سرطانی و سالم اشاره دارد. برخلاف سلولهای سالم که گلوکز را بهطور کامل به آب و دیاکسیدکربن تجزیه میکنند، سلولهای سرطانی گلوکز را تنها تا مرحلهی لاکتات میشکنند. این روند باعث تجمع بسیار بالای لاکتات در سلولهای سرطانی T گاه تا چهل برابر بیشتر از بافتهای سالم میشود.
شیائویانگ وو (Xiaoyang Wu)، استادیار مرکز پژوهش سرطان دانشگاه شیکاگو، میگوید: «هدف ما این بود که از این ویژگی شیمیایی منحصربهفرد برای شناسایی محل تومور و رهاسازی دارو تنها در آن ناحیه استفاده کنیم.»
برای تحقق این هدف، پژوهشگران از نانوذرات سیلیسی متخلخل بهره گرفتند؛ ذراتی بسیار ریز که میتوانند انواع داروها را درون خود جای دهند و از طریق جریان خون به نقاط مختلف بدن منتقل کنند. آنچه این سامانه را متمایز میکند، بهرهگیری از یک «سوییچ زیستی وابسته به لاکتات» است که فقط در محیطهای غنی از لاکتات – همچون بافتهای سرطانی – فعال میشود.
این سوییچ شامل دو بخش است: نخست، آنزیمی بهنام لاکتاتاکسیداز که لاکتات را به پراکسید هیدروژن تجزیه میکند، و دوم، مادهای شیمیایی حساس به پراکسید هیدروژن که همانند دری پوشاننده، مانع از آزاد شدن دارو میشود. در محیطهای سالم که لاکتات کمی دارند، این دری باقی میماند و دارو آزاد نمیشود؛ اما در اطراف سلولهای سرطانی، لاکتات بالا میرود، پراکسید هیدروژن تولید میشود، پوشش نانوذره از بین میرود و دارو بهطور هدفمند رها میشود.
بهگفتهی وو، طراحی این سامانه، گامی نوآورانه در ترجمهی سیگنال زیستیِ اختصاصی سرطان به یک واکنش شیمیایی فعال بوده است؛ موضوعی که پیشتر به دلیل خنثی بودن نسبی لاکتات، امکانپذیر نبوده.
در آزمایشهای پیشبالینی روی موشهای مبتلا به دو نوع سرطان، این سامانه موفق شد دُزی دهبرابر بیشتر از داروی رایج را به درون تومورها برساند، بدون آنکه به بافتهای سالم آسیبی وارد شود. این روش نهتنها سرعت رشد تومور را کاهش داد، بلکه بقا را نیز نسبت به تزریق مستقیم دارو افزایش داد.
از دیگر مزایای این فناوری آن است که میزان لاکتات در بیماران مبتلا به سرطان، با روشهای غیرتهاجمی همچون تصویربرداری رزونانس مغناطیسی (MRI) بهراحتی قابل سنجش است. این ویژگی میتواند بهعنوان معیاری برای انتخاب بیماران واجد شرایط در کارآزماییهای بالینی و پیشبینی اثربخشی درمان استفاده شود.
در نخستین گام، پژوهشگران این نانوذرات را با داروی دوکسوروبیسین، یکی از پرکاربردترین داروهای شیمیدرمانی، بارگذاری کردند. این دارو در درمان سرطان پستان، سارکوم، لنفوم و لوسمی کاربرد دارد. با این حال، نتایج امیدوارکنندهای در مورد بارگذاری دیگر داروهای شیمیدرمانی و ایمنیدرمانی نیز بهدست آمده است.
افزون بر سرطان، افزایش لاکتات در بیماریهایی همچون آرتریت نیز دیده میشود. از آنجا که داروهای ضدالتهاب سیستم ایمنی را سرکوب میکنند، بهکارگیری سامانهای که تنها در محیطهای خاص فعال میشود، میتواند عوارض جانبی این داروها را نیز کاهش دهد.
برای رساندن این فناوری به مرحلهی تولید صنعتی و کارآزمایی بالینی، دکتر وو با همکاری مرکز نوآوری پولسکی (Polsky Center) شرکت دانشبنیان «آلنیر درمانی» (Alnair Therapeutics) را بنیان نهاده است. وی میگوید چالش بعدی، تولید مقیاسپذیر این سامانه برای انسانهاست.
همچنین بر آن است تا دیگر تفاوتهای متابولیسمی میان سلولهای سرطانی و سلولهای سالم را شناسایی کرده و از آنها در طراحی سامانههای درمانی نوین بهره ببرد.